
在生物医学领域,mRNA作为一种极具潜力的治疗手段,正受到越来越多的关注。mRNA能够指导细胞合成特定的蛋白质,从而在治疗多种疾病方面展现出巨大的应用前景。然而,mRNA的纯化一直是制约其大规模生产和应用的关键难题之一。
mRNA分子带有负电荷,这使得阴离子交换层析成为一种有效的纯化手段。传统的阴离子交换层析通常适用于长度小于500个核苷酸(nt)的短mRNA。然而,当mRNA长度超过500nt时,由于其复杂的四级结构以及与固定相的强相互作用,使得洗脱回收变得极具挑战性。为了减弱这种强相互作用,通常需要在高温(约65°C)或添加变性剂的条件下进行操作。然而,在符合GMP的环境中实施高温解决方案面临着诸多困难。因此,开发一种能够在标准洗脱方法中实现高结合容量和高产量的纯化方法,成为了行业的迫切需求。
本文将介绍一种创新的阴离子交换层析方法,该技术不仅能够显著提高大分子mRNA的纯化效率和产量,还适用于大规模GMP生产环境。通过案例研究,我们将展示如何利用这一新型可线性放大的方法,有效去除双链RNA、聚集体及DNA/RNA等杂质,满足严格的产品质量要求。

研究方法与实验设计
在本研究中,研究人员采用了两种不同的洗脱技术——盐梯度洗脱和双重梯度洗脱,以评估其对mRNA纯化的效果。实验使用了Natrix® Q Micro 0.2 mL强阴离子膜层析装置。测试料液包括编码红细胞生成素(EPO)蛋白的mRNA(858nt)和编码萤火虫荧光素酶(FLuc)蛋白的mRNA(1,929nt)。
实验步骤如下表所示:
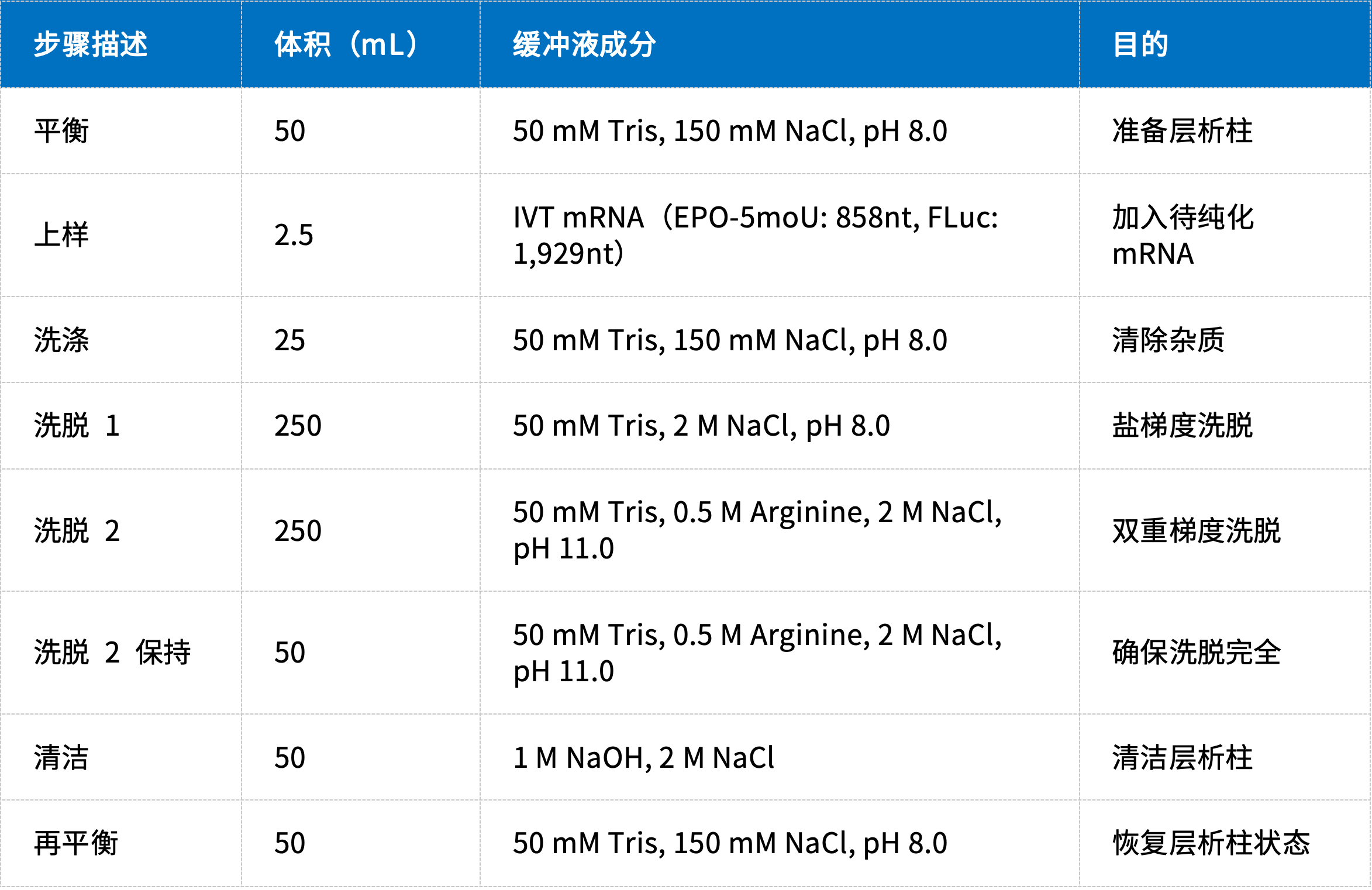

实验结果
如图1所示,对于858nt的mRNA EPO,部分mRNA在中性pH下通过NaCl梯度洗脱时能够被洗脱出来,但仍有部分mRNA仍然与Natrix® Q结合。相比之下,在0.5 M精氨酸作为混合盐的存在下,通过增加NaCl浓度和pH值,mRNA EPO能够被完全洗脱出来。
对于更长的1,929nt mRNA FLuc,由于其强氢键作用,通过NaCl梯度洗脱的效率较低,而双重梯度洗脱方法同样能够将其完全洗脱。不同长度的mRNA在层析操作过程中表现出相似的行为。除了主要的单链RNA(ssRNA)峰外,在双重梯度洗脱的后期还观察到了三个其他峰,这些可能是体外转录过程中产生的mRNA相关杂质。通过这种评估,双重梯度方法在室温下能够有效洗脱、高选择性地分离并去除大于800nt的RNA转录本中的杂质。
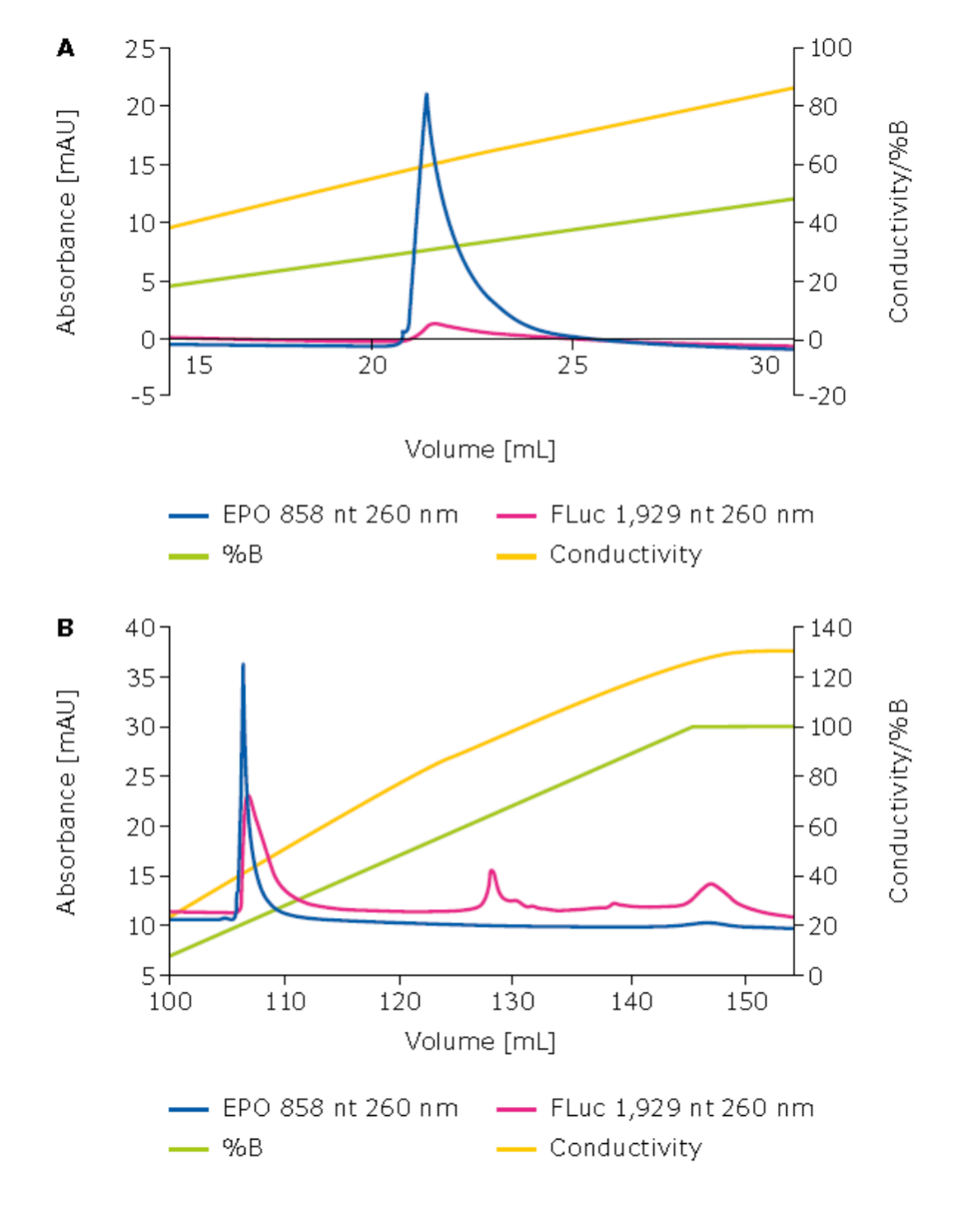
图1. 使用Natrix® Q Micro 0.2 mL对mRNA EPO(蓝色)和mRNA FLuc(粉色)的层析图谱对比
A. 在中性pH条件下,未添加混合盐的NaCl梯度洗脱
B. 在存在混合盐的情况下,通过增加pH值和盐浓度的双梯度洗脱
在实际生产中,通常更倾向于使用阶梯洗脱方法。为了模拟生产环境,研究人员应用了阶梯洗脱方法,并在各个分数中确定了mRNA的产量。实验结果显示,对于EPO(图2)和Fluc(图3),Natrix® Q总产量分别为92.6%和77.2%。尽管mRNA的长度不同,产量略有差异,尤其是FLuc mRNA由于含有较多杂质,导致其产量相对较低。即便如此,双重阶梯洗脱方法仍然能够保持较高的产量。
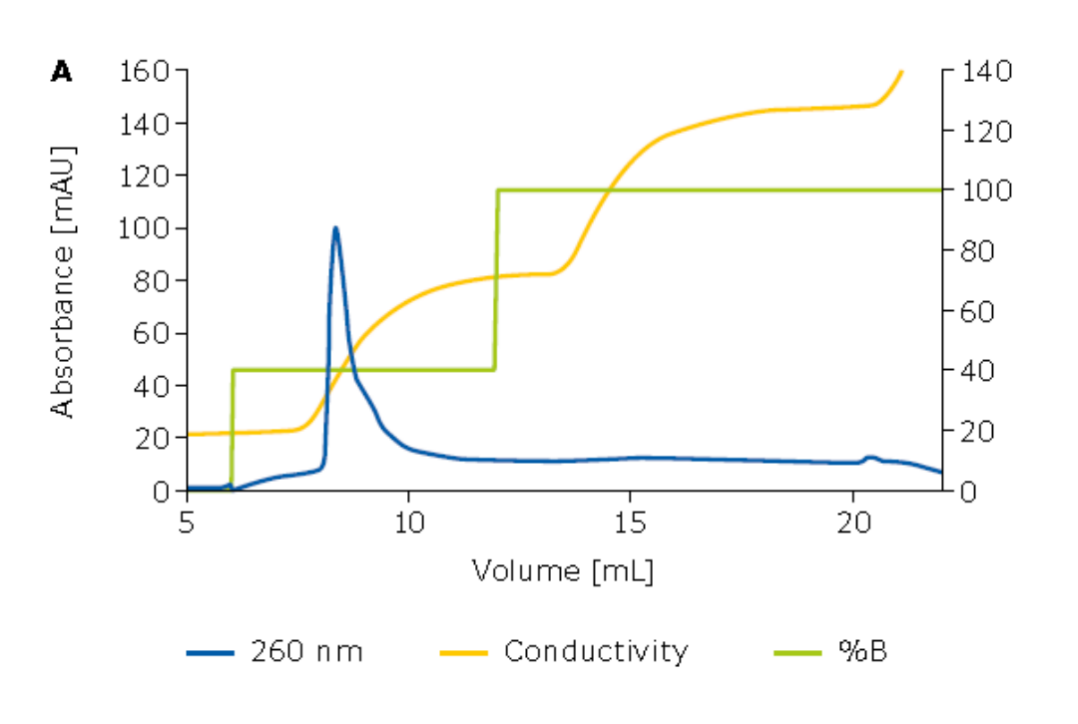
图2. 使用Natrix® Q 对mRNA EPO进行的阶段洗脱层析图谱
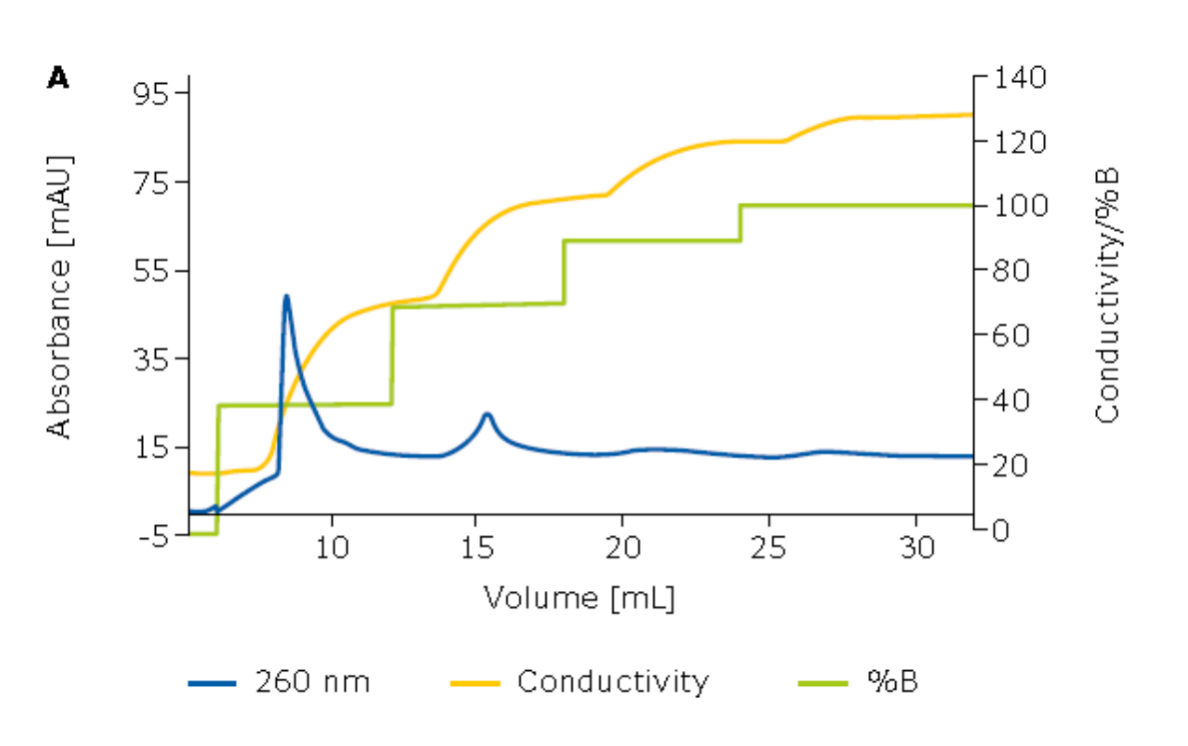
图3. 使用Natrix® Q 对mRNA Fluc进行的阶段洗脱层析图谱
为了确定杂质去除情况,使用dsRNA ELISA试剂盒定量了上样和洗脱液中的dsRNA水平。如图4所示,阴离子交换层析在dsRNA去除方面表现优异,去除率超过97%。
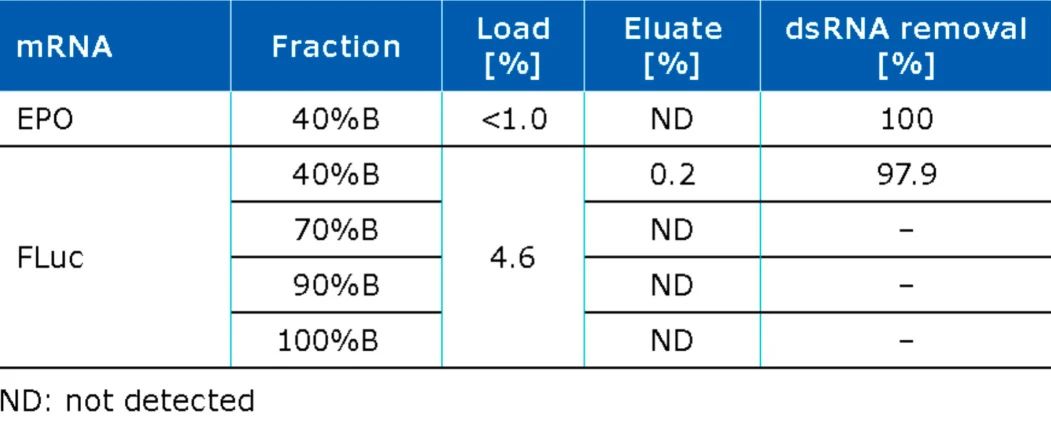
图4. dsRNA的质量平衡

关键结论
1. 最佳pH值、盐浓度和变性盐浓度协同作用,可提高mRNA从强阴离子交换剂中的洗脱性能。
2. 双重梯度洗脱方法:在混合盐存在的情况下同时增加pH值和盐浓度,能够实现高效mRNA洗脱,获得高产量,并有效分离dsRNA与ssRNA。
3. 无需在洗脱过程中提高温度,即可获得满意的回收率和纯度。
4. 这种新颖的可线性放大的方法能够在捕获和精制步骤中纯化更广泛的大型mRNA,并有望应用于mRNA治疗药物和疫苗的GMP生产。
Natrix® Q在本研究中的表现,不仅证明了其在mRNA纯化中的高效性和可靠性,还为未来的生物制药生产提供了一种新的、具有潜力的解决方案。Natrix® Q作为一种强阴离子交换膜层析产品,其配基为季铵基,具有高结合容量和良好的选择性,特别适用于处理复杂的生物分子。它在mRNA纯化中的应用,为解决上述挑战提供了一种新的思路。